В результате пре-скрининга у 74 из 248 пациентов метастатическим уротелиальным раком, были выявлены различные нарушения в генах, определяющих наличие DRD фенотипа (ATM, BRCA1, BRCA2, BRIP1, CDK12, CHEK2, FANCA, HDAC2, PALB2). После завершения индукционной химиотерапии 40 пациентов, завершивших индукционную химиотерапию (4-8 циклов) без признаков прогрессирования процесса, рандомизировались в 2 группы 1:1 (рис.1).
1. В первой группе больные получали рукапариб (600 мг х 2 раза в день)
2. Во второй группе – вместо рукапариба пациенты получали плацебо.
Рис.1 Дизайн исследования ATLANTIS

Первичной целью исследования была оценка выживаемости без прогрессирования, а вторичными целями – оценка общей выживаемости, частоты объективных ответов и переносимость терапии.
Приблизительно у 40% больных в обеих группах выявлялись висцеральные метастазы. Полный, частичный ответ и стабилизация на фоне индукционной химиотерапии были зарегистрированы у 30%, 60% и 10% больных соответственно.
В группе получавшей поддерживающую терапию рукапарибом были отмечены увеличение медианы выживаемости без прогрессирования с 15 до 35 недель (HR 0.53, 80% CI 0.30-0.92, p = 0.07) (рис.2) и тенденция к увеличению общей выживаемости (рис.3).
Рис.2. Выживаемость без прогрессирования
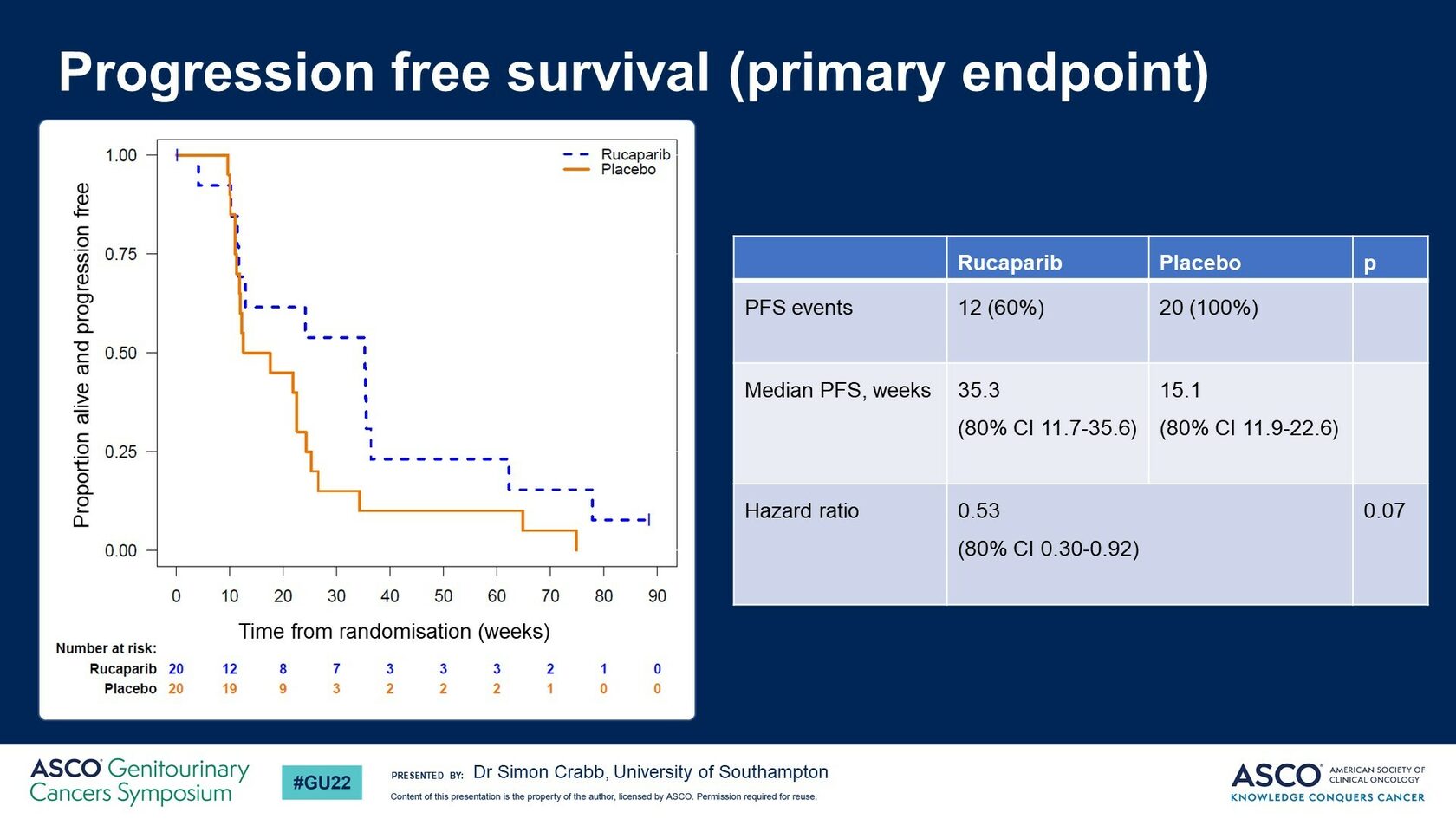
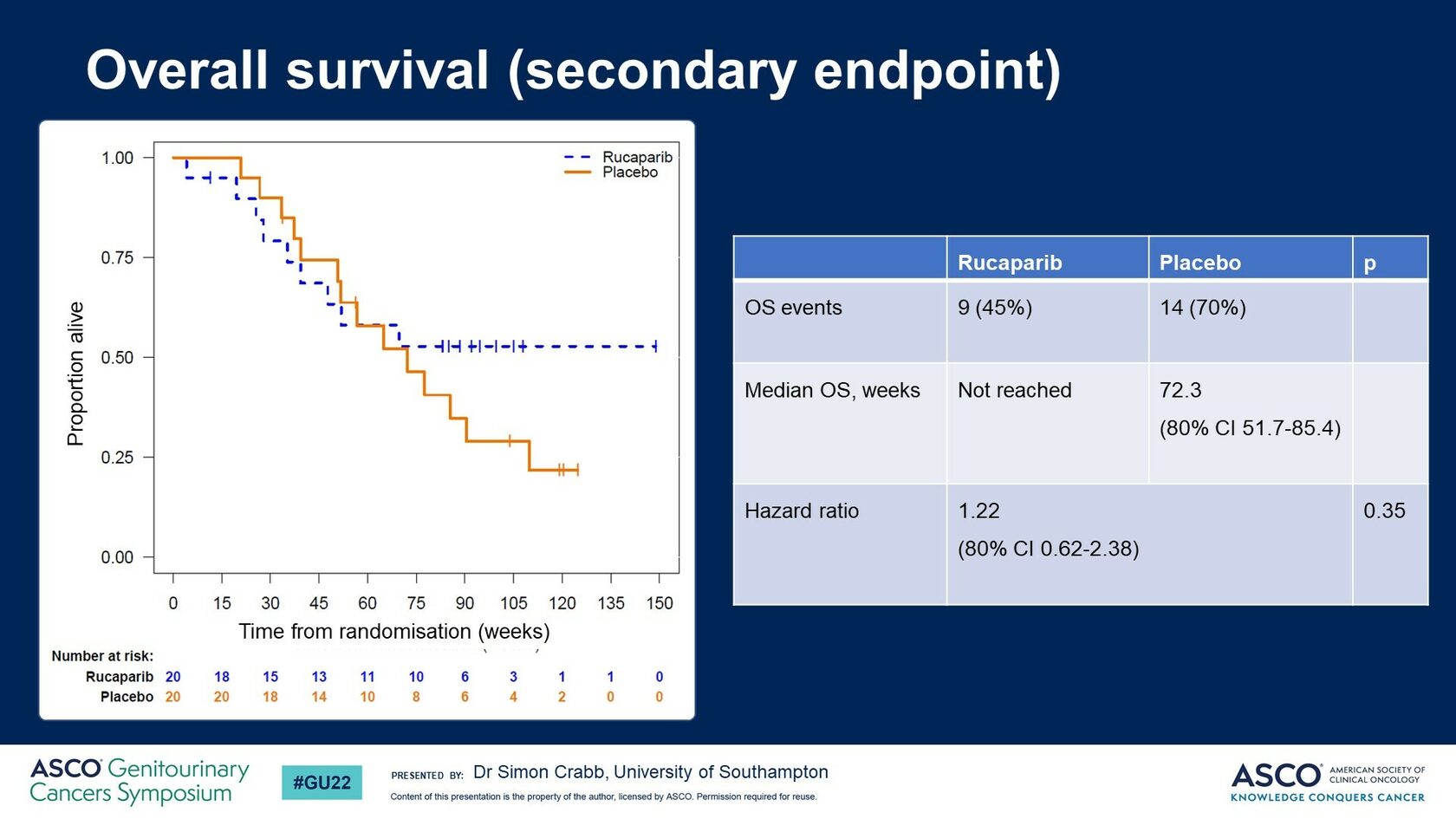
Рис.3 Общая выживаемость
Основными видами токсичности (1-4 ст.) были тошнота, сыпь и анорексия. Общая частота нежелательных явлений 3-4 ст. была небольшой и не превышала 5%.
Таким образом, авторы сделали вывод о возможной эффективности данного подхода и целесообразности изучения его в более крупном рандомизированном исследовании 3 фазы у пациентов с DRD фенотипом.
Ограничения. Пока недостаточно данных о клинической эффективности PARP ингибиторов в монорежиме у пациентов уротелиальноым раком. Небольшое число больных, получавших терапию в рамках данного клинического исследования. Необходимость отбора пациентов в зависимости от наличия у них DRD фенотипа.
