Рис.3. Выживаемость до развития инвазивных форм рецидива РМЖ у больных (pN1), в зависимости от вида адьювантной терапии и менопаузального статуса. (ET - гормонотерапия; CT+ET – химиотерапия+ГТ)
В декабрьском номере журнала NEJM были опубликованы очередные промежуточные результаты исследования RxPONDER [1], в котором исследователи попытались ответить на вопрос о целесообразности назначения адьювантной химиотерапии (ХТ) в дополнение к гормонотерапии пациенткам с люминальным B (Her2 негативным) подтипом рака молочной железы (РМЖ) и с поражением 1-3 регионарных лимфатических узлов (л/у) (pN1).
Ранее в другом исследовании TAILOR было доказано, что в популяции пациенток с pT1-2pN0 стадией РМЖ и промежуточным риском прогрессирования (RS=11-25 баллов) после радикального хирургического лечения, который определялся на основании уровня экспрессии 21 гена по шкале Oncotype DX (Breast Recurrence Score), только в возрастной группе <50 лет добавление адьювантной ХТ к гормональной терапии (ГТ) способствует достоверному увеличению 9-летней выживаемости без появления отдаленных метастазов. Данный показатель в абсолютных значениях увеличивался при риске прогрессирования RS 16-20 всего на 1.5%, а при RS 21-25 баллов – уже на 6.5% [2].
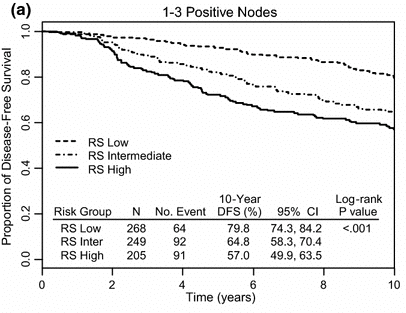
Оставалось не очень понятно, какую пользу от ХТ получают пациентки с невысоким риском рецидива (RS 0-25 баллов) при ограниченном поражении л/у (1-3 л/у). В исследовании NSABP B-28 было продемонстрировано, что данная популяция больных также представляется достаточно неоднородной с точки зрения риска развития рецидива, определяемого по шкале Oncotype DX ( (рис.1) [3].
Рис.1. Выживаемость без прогрессирования в популяции больных HR+ Her2-негатив РМЖ pN1 стадией (1-3 пораженных регионарных л/у) в зависимости от риска рецидива, определяемого по шкале Oncotype DX (Breast Recurrence Score).
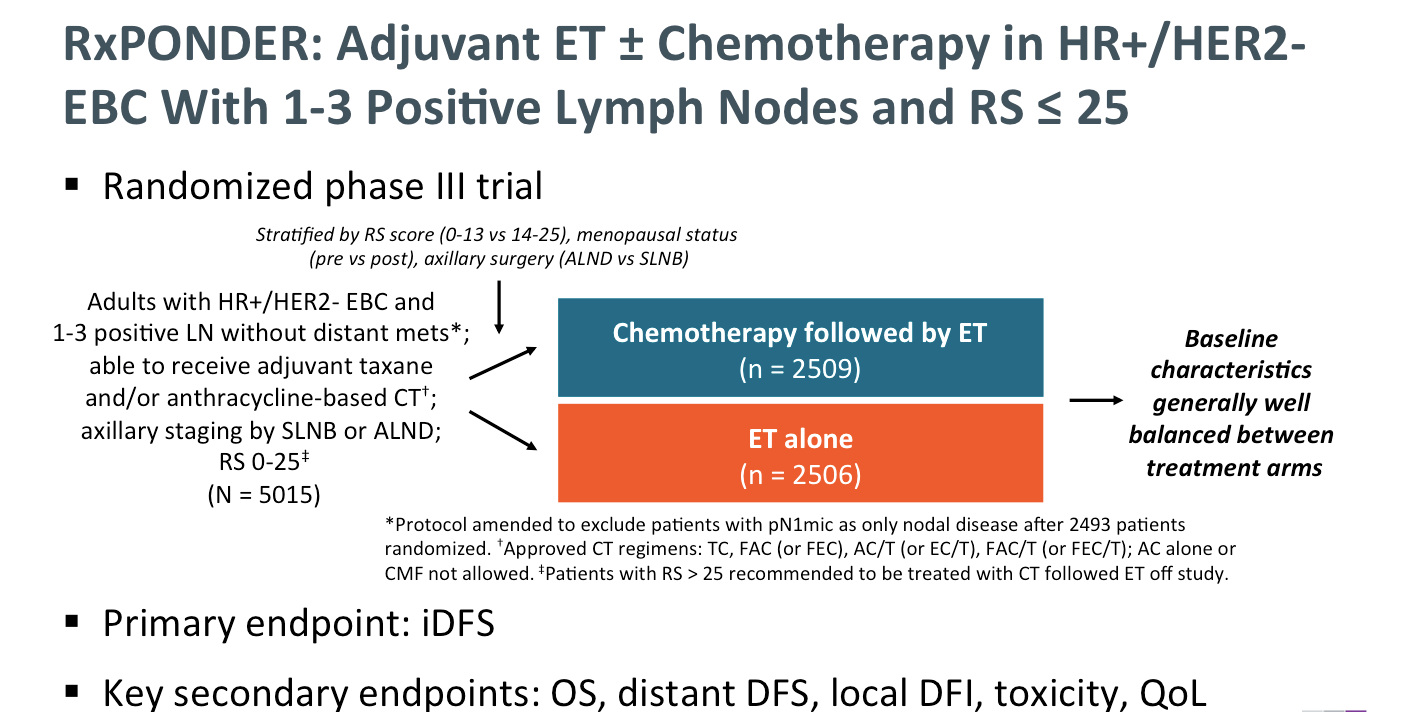
В новом исследовании RxPONDER в общей сложности 5083 пациентки HR+ Her2-negative с pN1 стадией (поражение 1-3 регионарных л/у) были рандомизированы в 2 группы. В первой группе проводилась только гормональная терапия, во второй – ХТ и ГТ в соответствии с установленными стандартами (рис.2). В исследовании преобладали постменопаузальные больные (33.2% пременопаузальные и 66.8%).
Рис.2. Дизайн исследования RxPONDER
Основной целью исследования была оценка выживаемости до развития инвазивных форм РМЖ. Вторичной целью – сравнение выживаемости до развития отдаленных метастазов и общей выживаемости.
В популяции постменопаузальных пациенток добавление ХТ к ГТ не снижало риск развития инвазивного рецидива РМЖ (HR=1.02; 95% CI, 0.82 to 1.26; P=0.89) и не улучшало 5-летнюю выживаемость без инвазивного рецидива – 91.9% и 91.6% в группе ГТ и ХТ+ГТ соответственно (рис.3). При этом, в популяции пременопаузальных больных, данные показатели были достоверно лучше в группе ХТ+ГТ. Проведение адьювантной ХТ с последующей ГТ позволило снизить как риск до развития инвазивных форм рецидива (HR 0.60; 95% CI, 0.43 to 0.83; P=0.002), так и риск развития отдаленных метастазов на 5.0% (HR 0.58; 95% CI, 0.39 to 0.87; P=0.009).
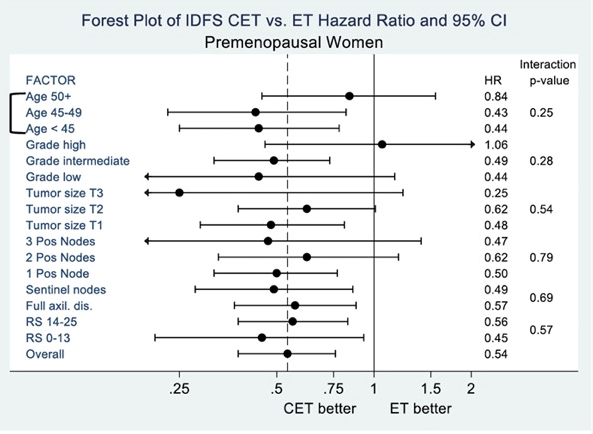
Но в этой же пременопаузальной популяции больных польза от добавления ХТ была ограничена только возрастной группой моложе 50 лет (HR 0.48; 95% CI = 0.32–0.72) (рис.4). Пациентки старше 50 лет, находящиеся в пременопаузе, не выигрывали от добавления адьювантной ХТ к ГТ.
Рис.4. Подгрупповой анализ (forest plot) риска развития инвазивных форм рецидива у больных в пременопаузе в зависимости от вида адьювантной терапии.
Авторы сделали вывод, что в популяции больных РМЖ pN1 стадией (1-3 пораженных регионарных л/у) и RS 0-25 проведение адьювантной ХТ с последующей ГТ позволяет снизить риск рецидива только у пациенток в пременопаузе. Для пациенток, находящихся в постменопаузе, адьювантная ГТ является вполне достаточной с точки зрения ее эффективности.
Ограничения и вопросы для дальнейшего изучения
Критерии включения не предусматривали оценку результатов адьювантной терапии у пациенток с низким риском рецидива РМЖ по шкале Oncotype DX (RS 0-25) и с pN2 стадией. Поэтому не совсем понятно, чем отличаются биологические характеристики РМЖ с низким риском по шкале Oncotype DX (RS 0-25) при стадии pN2 и pN1? Также остается не ясным получат ли постменопаузальные пациентки РМЖ pN1 стадией и RS немногим выше 25 (например, RS 25-30), какую-либо пользу от добавления ХТ к ГТ?
Почему среди пациенток в премонапаузе (pN1 и RS 0-25) только больные моложе 50 лет выигрывают от добавления ХТ к ГТ, а больные старше 50 лет нет? Возможно, что основной противоопухолевой эффект в этой популяции реализуется через овариальную супрессию, достигаемую за счет адьювантной ХТ. Данная гипотеза должно быть предметом дальнейшего изучения в клинических исследованиях.
1. Kalinsky K, Barlow WE, Gralow JR, et al: 21-gene assay to inform chemotherapy benefit in node-positive breast cancer. N Engl J Med 385:2336-2347, 2021.
2. Sparano JA, Gray RJ, Makower DF, et al: Adjuvant chemotherapy guided by a 21-gene expression assay in breast cancer. N Engl J Med 379:111-121, 2018.
3. Eleftherios P. Gong T., Soonmyung P. et al. 21‑Gene Recurrence Score for prognosis and prediction of taxane benefit after adjuvant chemotherapy plus endocrine therapy: results from NSABP B‑28/NRG Oncolog. Breast Cancer Res Treat (2018) 168:69–77.
